傳媒
上一頁
港大理學院金屬蛋白研究 助抑制幽門螺旋菌突變
2010年03月05日
|
在與人類對抗的過程中,病菌往往通過快速變異令藥物產生耐藥性,令投入臨床使用的藥物很快便失效。香港大學化學系研究小組,透過現代系統科學的新方法,對金屬化合物(metal complexes)(特別是鉍(bismuth)等含非生命必需金屬的化合物)所導致的有機體敏感展開深入研究,發現含鉍的抗炎藥物,可抑制幽門螺旋菌突變,延緩病菌的耐藥性。而此研究基理,亦可應用於其他病菌研究之上。其成果剛於2010年3月初在世界著名的多學科刊物《美國國家科學院院刊》(Proceedings of National Academy of Sciences of the United States of America)中發表(www.pnas.org )。 目前,新型抗生素的研發可謂憂喜參半。一方面,研究人員透過干擾致病蛋白質和特定金屬的相互作用,達到治療效果;另一方面,病菌很快便適應有機類抗生素,產生耐藥性,令其失去療效。雖然金屬類抗生素被廣泛應用,但研究人員還需對其作用及機理深入了解,才能進一步提高療效及延長使用壽命。最近,港大化學系孫紅哲教授與寸樹健博士採用化學生物學結合金屬組學的方法,對寄生於消化道中的幽門螺旋桿菌進行研究,發現此病菌中一種不可或缺的蛋白質GroES發生了罕見的變異─其結構頂部產生了一個可與金屬鋅(Zinc)結合的位點,令病菌突變生長。此位點的形成,很可能出於生物進化中的負向選擇(negative selection)。實驗指出,含鉍的抗炎藥物可與此位點強力結合,取代原有的鋅,破壞蛋白質的整體結構,從而抑制細菌生長。一般而言,產生於負向選擇的生物學特性難以迅速突變,所以研究成果揭示出一種極有潛力的藥物研發途徑─通過抑制病菌在進化中所形成的特性,將可達致治療目的,同時延緩耐藥性的出現。 孫教授和其團隊研究金屬於生物學、醫學上的應用達十年之久,致力為無機化學與化學生物學研究開拓新領域。他們正計劃將是次發現的藥物作用機理擴展於其他病菌研究之上,了解在病菌中是否存在普遍的負向選擇特性,從而設計新型的或改良現有的藥物,以延緩病菌耐藥性,並增加治愈疾病的機會。此金屬蛋白研究,乃獲香港特別行政區政府轄下研究資助局的「合作研究基金」資助下所進行。 過往孫教授亦曾與港大李嘉誠醫學院的研究小組合作,共同研發可抑制嚴重急性呼吸道綜合症(SARS)的藥劑,當中包括一種臨床使用中的藥物。此藥物針對病毒中一種酶(enzyme)的金屬結合位點進行攻擊,從而阻斷病毒複製以控制病情。 傳媒如有垂詢,可致電香港大學理學院傳訊經理陳詩迪小姐(電話:2241 5286/ 6356 5626)或電郵至cindycst@hku.hk 有關《美國國家科學院院刊》 《美國國家科學院院刊》(Proceedings of the National Academy of Sciences of the United States of America,通常簡稱為PNAS)是美國國家科學院的官方科學周刊雜誌。雜誌於於1915年創刊,出版世界各地從事基礎科學領域研究人員的的報告、述評、和論文等。該刊覆蓋的領域甚廣,包括生物學、物理學、數學和社會科學等。 有關負向選擇 在進化的過程中,生物分子以隨機的方式產生突變。其中一部分可能對其功能產生不利的影響,這樣的突變通常被自然選擇所淘汰,不久後即在後代中消失,稱作「負向選擇」。但在某些情況下,此類突變所導致的生理特性會被一些生活在環境特殊中的生物(如寄生病菌)所利用,以適應其特殊的生活方式。 |
 港大化學系孫紅哲教授(左)與寸樹健博士 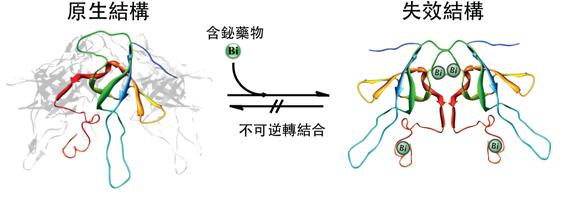 病菌蛋白質在含鉍複合物作用下發生結構解體 |
