傳媒
港大發現核糖核酸(RNA)編輯為新致癌原因
RNA編輯可逆轉 肝癌治療有希望
2013年01月28日
香港大學李嘉誠醫學院臨床腫瘤學系腫瘤遺傳實驗室首度發現核糖核酸(RNA)編輯現象會令正常細胞變成癌細胞,導致罹患肝癌。科學家早已發現基因突變是癌症其中一種成因,但由於目前已知攜帶特定基因突變而致癌的病人只佔小部分,而RNA編輯特定基因則會影響大多數病人,加上基因突變不能逆轉,但RNA編輯則是可以調控,因此,本研究為癌症治療及標靶藥物發展帶來重要突破及新方向。有關研究成果最近已於頂尖學術期刊《自然—醫學》(Nature Medicine)上發表。
負責研究的香港大學李嘉誠醫學院臨床腫瘤學系關新元教授說:「癌症研究一般著重基因突變對腫瘤形成的影響,忽略RNA編輯所起的作用。其實基因突變和RNA編輯造成的後果相似,兩者均可能令蛋白質序列和功能起變化。由於攜帶特定基因突變而致癌的病人只佔小部分,而RNA編輯特定基因則會影響大多數病人,所以我們相信針對RNA編輯而設計的標靶治療藥物對大部分肝癌病人能夠發揮療效。」
關於RNA編輯
基因決定人體構造的各項特性,而這些基因的資訊則儲存在遺傳物質—去氧核糖核酸(DNA)裡面。RNA扮演運送的媒介,負責將DNA裡的資訊傳遞到合成蛋白質的工廠裡面,指導蛋白質的合成。最後由蛋白質執行身體所需的各種功能。過程中,DNA內儲存的資訊變異、資訊抄寫到RNA時出現的錯誤或沒有按圖紙製造蛋白質等原因,都有可能造成細胞的性質、狀態或功能出現異常。RNA編輯是指在某些情況下,DNA的資訊即使正確地抄寫到RNA上,但卻在抄寫完畢後進一步被編輯,RNA編輯有機會因而改寫了RNA上的資訊,導致製造蛋白質過程出現變異。然而,RNA編輯在過程中如何發揮作用和其影響至今仍然是一個謎。
研究方法及成果
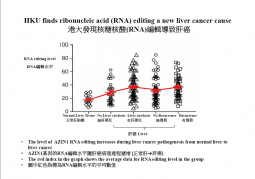
港大研究人員為解開謎團,利用新一代基因組外顯子測序技術(Transcriptome Sequencing Technology)對RNA進行搜索。他們將200個本港及內地肝癌病人樣本,利用體外培植肝癌細胞進行試驗分析及研究,並同時在實驗小鼠進行模擬實驗。結果發現,一種名為AZIN1的基因經常進行RNA編輯,但它們在正常的肝臟、血液以及其他器官內幾乎檢測不到或只能低頻率地檢測到編輯現象。研究進一步揭示,肝臟細胞內負責RNA編輯的機器ADAR1失靈,導致錯誤地高頻率編輯AZIN1基因。RNA編輯因而改變了AZIN1的蛋白編碼序列,很可能引發蛋白質出現構造上的變化,繼而造成AZIN1蛋白質功能變異。臨床病理資料顯示,RNA編輯與肝硬化、肝癌復發及存活期短等緊密相關。今次研究亦證實,RNA編輯能導致正常肝細胞轉化成癌細胞。研究團隊相信若然能夠及時修復失靈的RNA編輯機器,或改寫被錯誤編輯的AZIN1基因,都有可能逆轉正常肝細胞轉化成癌細胞的情況。
研究啟示
今次研究是全球首次證實AZINI基因的RNA編輯能導致癌症發生。其在科學領域有著重大的意義,它引領我們從一個新角度去審視癌症發生的機理,相信會引起研究RNA編輯的熱潮,更有望為肝癌甚至更多的癌症提供嶄新而有效的標靶治療發展方向。相對那些不可逆轉的基因突變,RNA編輯是可調控、可逆轉的表觀遺傳學過程。針對表觀遺傳學機制研發的臨床藥物正是當今醫藥界的熱點,它為患者帶來了新的希望,骨髓增生異常綜合症是當中成功的例子。
關於肝癌
肝癌是指發生於肝臟的惡性腫瘤,是臨床上最常見的惡性腫瘤之一。根據香港衞生署的統計, 2009年全港肝癌新症數目約有1800宗,死亡人數約1500多人,位居香港致命腫瘤的第三位。全球每年有超過五十萬宗新症,國內發病人數更佔全球半數以上。手術切除腫瘤是目前治療早期肝癌的最好辦法,但由於肝癌早期一般缺乏典型及明顯的徵狀,所以病人往往在中晚期才被確診。又因肝腫瘤惡性度高、病情惡化速度快,故此治療難度大、療效差,一般發病後存活期僅為六到二十個月。
研究隊伍
這項研究由香港大學臨床腫瘤學系癌症研究實驗室關新元教授領導,新加坡國立大學癌症科學中心合作完成。其他主要研究人員包括香港大學博士後研究生陳蕾蕾、李妍及新加坡國立大學癌症科學中心DG Tenen教授。本研究獲香港研究資助局多項科研經費資助。
如欲瀏覽新聞圖片,請登入以下網址:http://www.med.hku.hk/v1/news-and-events/press-releases/